Reaksiyong kimikal
Ang reaksiyong kimikal ay isang proseso ng nagreresulta sa isang pagpapalitan ng mga sustansiyang kimikal [1]. Tinatawag na mga reaktiboo nagbibigay ng reaksyong ang sustansiya o mga sustansiya na unang nasangkot na reaksiyong kimikal. Tinatangi ang mga reaksiyong kimikal sa pamamagitan ng pagbabagong kimikal at nagbubunga ito ng isa o higit pa na mga produkto na naiiba sa mga reaktibo. Sa kadalasan, sinasakop ng mga reaksiyong kimikal ang mga pagbabago na mahigpit na kinakasangkutan ng mga paggalaw ng mga elektron sa pabubuo at pagwasak ng mga kawing kimikal, bagaman nailalapat ang pangkalahatang konsepto ng isang reaksiyong kimikal, partikular ang kuro-kuro sa isang ekwasyong kimikal, sa mga pagbabago ng pangunahing mga maliit na bahagi, gayon din ng mga reaksiyong nukleyar.
Sa klasikal na konteksto, ang reaksyong kimikal ay sumasakop sa mga pagbabago na may kinalaman lamang sa mga posisyon ng mga elektron sa pagbuo at pagsira ng mga ugnayang kimikal sa pagitan ng mga atomo, na walang kasamang pagbabago sa nukleyo (walang pagbabago sa elementong kabilang), at maaaring madalas nating tawaging ekwasyong kimikal. Ang kimikang nukleyar ay isang sangay ng kimika na may kinalaman sa mga reaksyong kimikal ng mga di-matatag at radyoaktibong elemento kung saan parehong elektroniko o nukleyar na pagbabago ang maaaring maganap.
Ang sangkap (o mga sangkap) sa simula na may kinalaman sa isang reaksyong kimikal ay tinatawag na mga reaktibo o reagent. Ang mga reaksiyong kimikal ay karaniwang nailalarawan sa pamamagitan ng pagbabagong kimikal, at nagbibigay ang mga ito ng isa o higit pang produkto na karaniwang may mga katangiang iba mula sa mga reaktibo. Ang mga reaksyon ay kadalasang binubuo ng mga sunod-sunod na indibiduwal na hakbang, na siya nating tinatawag na elementarya reaksyon, at ang mga impormasyon mula sa tiyak na hakbangin ay bahagi ng mekanismong reaksyon. Ang mga reaksyong kimikal ay nailalarawan sa mga ekwasyong kimikal, na kung saan grapikal na maipapakita ang mga paunang materyales, mga dulong produkto, at kung minsan ay ang mga gitnang produkto at mga kondisyon ng reaksyon.
Ang mga reaksiyong kimikal ay nagaganap sa katangi-tanging bilis ng reaksyon sa isang nakasaad na temperatura at konsentrasyong kemikal. Ang mga mabilisang reaksyon ay tinatawag na likas, na hindi na nangangailangan ng iba pang uri ng dagdag na enerhiya maliban sa enerhiyang nagmumula sa init. Ang mga hindi likas na reaksyon ay mabagal ang proseso. Sila ay mga prosesong nangangailangan ng iba pang-uri ng dagdag na enerhiya (dagdag na init, liwanag, elektrisidad) upang matapos at mabalanse ang reaksyon sa parehong antas ng likas na reaksyon.
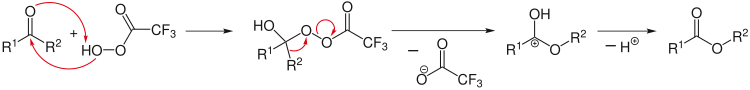
Mga reaksyong elementarya
baguhinAng reaksyong elementarya ay ang pinakamaliit na dibisyon kung saan maari ihiwalay reaksyong kimikal, wala itong mga produktong intermediya.[2] Ginagawa ang karamihan sa mga reaksyong minamasid sa eksperimento mula sa maraming mga reaksyong elementarya na nangyayari ng kaagapay o sunod-sunod. Tinatawag na mekanismong reaksyon ang aktuwal na pagkakasunod-sunod ng indibiduwal na mga reaksyong elementarya. Kinakasangkutan ng iilang mga molekula ang isang reaksyong elementarya, na kadalasang isa o dalawa, dahil mababa ang probabilidad para sa ilang molekula na magsalubong sa isang tiyak na oras.[3]
Prekursor
baguhinSa kimika, ang prekursor ay isang kompuwesto na nakikilahok sa isang reaksyong kimikal na lumilikha ng isa pang kompuwesto. Sa biyokimika, ang terminong prekursor ay espesipikong ginagamit upang tukuyin ang isang kemikal na kompuwesto na nauuna sa isang metabolikong landas.
Mga sanggunian
baguhin- ↑ "Kahulugan ng chemical reaction sa IUPAC (sa Ingles)" (PDF). Inarkibo mula sa orihinal (PDF) noong 2009-09-30. Nakuha noong 2006-05-02.
{{cite web}}: CS1 maint: date auto-translated (link) - ↑ IUPAC, Compendium of Chemical Terminology, Ika-2 ed. (ang "Gold Book") (1997). Naitamang online na bersyon: (2006–) "elementary reaction". doi:10.1351/goldbook.E02035 (sa Ingles)
- ↑ Frenking, Gernot (2006). "Elementarreaktionen". Römpp Chemie-Lexikon (sa wikang Ingles). Thieme.
{{cite ensiklopedya}}: CS1 maint: date auto-translated (link)