Sodium bicarbonate
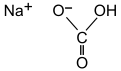
Ang sodium bicarbonate (Kastila: bicarbonato de sodio), na kilala rin bilang sodang panghurno (Ingles: baking soda), ay isang kompuwestong kimikal na may pormulang NaHCO3. Isa itong asin na binubuo ng sodyong kasyon (Na+) at bikarbonatong anyon (HCO3−). Isang puting solido ang sodium bicarbonate na malakristal, ngunit pinong pulbos ang kadalasang itsura nito. Mayroon itong bahagyang maalat, alkalinang lasa ng kahawig sa sodium carbonate. Nahcolite ang tawag sa anyong likas na mineral nito. Isa itong bahagi ng mineral na natron at masusumpungan ito na nakatunaw sa maraming bukal.[9]
| |||
| |||

| |||
| Mga pangalan | |||
|---|---|---|---|
| Pangalang IUPAC
sodium hydrogencarbonate
| |||
| Mga ibang pangalan
Sodang panghurno, baking soda
| |||
| Mga pangkilala | |||
Modelong 3D (JSmol)
|
|||
Reperensya sa Beilstein
|
4153970 | ||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Infocard ng ECHA | 100.005.122 | ||
| Bilang ng EC |
| ||
| Bilang ng E | E500(ii) (mga regulador ng pagkaasido, ...)]] | ||
| KEGG | |||
| MeSH | Sodium+bicarbonate | ||
PubChem CID
|
|||
| Bilang ng RTECS |
| ||
| UNII | |||
Dashboard ng CompTox (EPA)
|
|||
| |||
| |||
| Mga pag-aaring katangian | |||
| NaHCO3 | |||
| Bigat ng molar | 84.0066 g mol−1 | ||
| Hitsura | Puting kristal | ||
| Amoy | Walang amoy | ||
| Densidad |
| ||
| Puntong natutunaw | (Decomposes to sodium carbonate starting at 50 °C[1][6]) | ||
Solubilidad sa tubig
|
|||
| Solubilidad | 0.02 wt% acetone, 2.13 wt% methanol @22 °C.[4] insoluble in ethanol | ||
| log P | −0.82 | ||
| Pagkaasido (pKa) | |||
Repraktibong indeks (nD)
|
nα = 1.377 nβ = 1.501 nγ = 1.583 | ||
| Termokimika | |||
Kakayahan ng init (C)
|
87.6 J/mol K[7] | ||
Pamantayang entropiyang
molar (S⦵298) |
101.7 J/mol K[7] | ||
Pamantayang entalpya
ng pagbuo (ΔfH⦵298) |
−950.8 kJ/mol[7] | ||
Enerhiyang malaya na Gibbs (ΔfG⦵)
|
−851.0 kJ/mol[7] | ||
| Parmakolohiya | |||
| B05CB04 (WHO) B05XA02, Padron:ATCvet | |||
| Mga panganib | |||
| Kaligtasan at kalususgan sa trabaho (OHS/OSH): | |||
Pangunahing peligro
|
Nagdudulot ng malubhang pangangati sa mata | ||
| NFPA 704 (diyamanteng sunog) | |||
| Punto ng inplamabilidad | Di-nasusunog | ||
| Nakakamatay na dosis o konsentrasyon (LD, LC): | |||
LD50 (dosis na panggitna)
|
4220 mg/kg (rat, oral)[8] | ||
| Dokumento ng datos ng kaligtasan (SDS) | External MSDS | ||
| Mga kompuwestong kaugnay | |||
Ibang mga anion
|
Sodium carbonate | ||
Ibang mga cation
|
|||
Mga kaugnay na kompuwesto
|
|||
Maliban kung saan nabanggit, binigay ang datos para sa mga materyales sa kanilang estadong pamantayan (sa 25 °C [77 °F], 100 kPa).
| |||

Paggamit
baguhinPagluluto
baguhinPampaalsa
baguhinSa pagluluto, pangunahing ginagamit ang sodang panghurno sa paghuhurno bilang pampaalsa. Kapag may reaksiyon ito sa asido, lumalabas ang carbon dioxide, kaya umaalsa ang batter at nabubuo ang kilalang tekstura at ligasgas sa mga cake, tinapay, at iba pang pagkaing inihuhurno at ipiniprito. Maaaring katawanin ang reaksiyong asido–base ng sumusunod:[10]
- NaHCO3 + H+ → Na+ + CO2 + H2O
Kabilang sa mga asidong materyales na nag-uudyok ng ganitong reaksiyon ang mga hydrogen phosphate, krema ng tartar, katas ng limon, yogurt, buttermilk, cocoa, at suka. Maaaring gamitin ang sodang panghurno sa maasidong sourdough, para gumaan ito at mabawasan ang maasidong lasa nito.[11]
Maaari ring pakilusin ng init mismo ang sodium bicarbonate bilang pampaalsa sa paghuhurno dahil sa dekomposisyong termal, at lumalabas ang carbon dioxide sa mga temperaturang higit sa 80 °C (180 °F), gaya ng sumusunod:[12]
- 2 NaHCO3 → Na2CO3 + H2O + CO2
Kapag ginamit sa ganitong paraan na mag-isa, nang walang maasidong sangkap (sa batter man o sa paggamit ng pulbos panghurno na may nilalamang asido), kahalati lamang ng CO2 ang lumalabas (isang molekula ng CO2 ang nabubuo sa bawat dalawang katumbas na NaHCO3). Bukod pa rito, sa kawalan ng asido, ang dekomposisyong termal ng sodium bicarbonate ay nagluluwal din ng sodium carbonate, na napakaalkalina at nagbibigay ng mapait at masabon na lasa at dilaw na kulay sa inihurnong produkto. Dahil mabagal ang reaksiyon sa temperatura ng silid, maaaring ipatayo ang mga halo (cake batter, atbp.) nang hindi umaalsa hanggang pinainit sa hurno.[kailangan ng sanggunian]
Pulbos panghurno
baguhinNaglalaman ang pulbos panghurno, na ibinebenta rin sa pagluluto, ng halos 30% ng bikarbonato, at iba't ibang maasidong sangkap na naaaktiba sa pagdagdag ng tubig nang hindi kailangan ng karagdagang asido sa pinaglulutuan.[13][14][15] Maraming anyo ng pulbos panghurno ang naglalaman ng sodium bicarbonate na pinagsama sa calcium acid phosphate, sodium aluminum phosphate, o krema ng tartar.[16] Alkalina ang sodang panghurno; hindi nagkakaroon ng lasang metal ang asido na ginagamit sa pulbos panghurno kapag naglilikha ng sodium carbonate ang kemikal na pagbabago sa paghuhurno.[17]
Mga sanggunian
baguhin- ↑ 1.0 1.1 Haynes, p. 4.90
- ↑ 2.0 2.1 2.2 Haynes, p. 5.194
- ↑ 3.0 3.1 3.2 "Sodium Bicarbonate" [Sodyo Bikarbonato] (PDF) (sa wikang Ingles). United Nations Environment Programme. Inarkibo mula sa orihinal (PDF) noong Mayo 16, 2011.
{{cite web}}: CS1 maint: date auto-translated (link) - ↑ Ellingboe JL, Runnels JH (1966). "Solubilities of Sodium Carbonate and Sodium Bicarbonate in Acetone-Water and Methanol-Water Mixtures" [Mga Solubilidad ng Sodyo Karbonato at Sodyo Bikarbonato]. J. Chem. Eng. Data (sa wikang Ingles). 11 (3): 323–324. doi:10.1021/je60030a009.
{{cite journal}}: CS1 maint: date auto-translated (link) - ↑ 5.0 5.1 Haynes, p. 7.23
- ↑ Pasquali I, Bettini R, Giordano F (2007). "Thermal behaviour of diclofenac, diclofenac sodium and sodium bicarbonate compositions". Journal of Thermal Analysis and Calorimetry. 90 (3): 903–907. doi:10.1007/s10973-006-8182-1. S2CID 95695262.
{{cite journal}}: CS1 maint: date auto-translated (link) - ↑ 7.0 7.1 7.2 7.3 Haynes, p. 5.19
- ↑ Chambers M. "Sodium bicarbonate [USP:JAN]". ChemIDplus. U.S. National Library of Medicine.
- ↑ "Mineral Springs – an overview | ScienceDirect Topics" [Bukal – isang sumaryo] (sa wikang Ingles).
- ↑ Bent AJ, pat. (1997). The Technology of Cake Making [Ang Teknolohiya sa Paggawa ng Keyk] (sa wikang Ingles) (ika-6 (na) edisyon). Springer. p. 102. ISBN 9780751403497. Nakuha noong Agosto 12, 2009.
{{cite book}}: CS1 maint: date auto-translated (link) - ↑ Cascio J. "Sourdough" (PDF) (sa wikang Ingles). University of Alaska Fairbanks Cooperative Extension Service. FNH-00061. Inarkibo mula sa orihinal (PDF) noong Marso 27, 2016. Nakuha noong Mayo 2, 2017.
{{cite web}}: CS1 maint: date auto-translated (link) - ↑ "The Many Practical Uses of Baking Soda in the Kitchen" [Ang Maraming Pratikal na Paggamit ng Sodang Panghurno sa Kusina]. About.com Food (sa wikang Ingles). Inarkibo mula sa orihinal noong Pebrero 2, 2017. Nakuha noong Enero 22, 2017.
{{cite news}}: CS1 maint: date auto-translated (link) - ↑ Czernohorsky JH, Hooker R. "The Chemistry of Baking" [Ang Kimika ng Paghuhurno] (PDF) (sa wikang Ingles). New Zealand Institute of Chemistry. Inarkibo mula sa orihinal (PDF) noong Nobyembre 27, 2016. Nakuha noong Enero 22, 2017.
{{cite web}}: CS1 maint: date auto-translated (link) - ↑ "Baking Soda and Baking Powder" [Sodang Panghurno at Pulbos Panghurno]. FineCooking.com (sa wikang Ingles). Inarkibo mula sa orihinal noong Pebrero 2, 2017. Nakuha noong Enero 22, 2017.
{{cite news}}: CS1 maint: date auto-translated (link) - ↑ "Baking Soda FAQs" [Mga Madalas Itanong sa Sodang Panghurno]. Arm & Hammer Multi-Brand (sa wikang Ingles). Church & Dwight Company. What is the difference baking soda and baking powder?. Inarkibo mula sa orihinal noong 27 Hunyo 2017. Nakuha noong 20 Hulyo 2017.
{{cite web}}: CS1 maint: date auto-translated (link) - ↑ "Glossary Ingredients". Cooking.com. Inarkibo mula sa orihinal noong 15 Setyembre 2008.
{{cite web}}: CS1 maint: date auto-translated (link) - ↑ "Sodium Bicarbonate" [Sodyo Bikarbonato]. BRP Adhikary (sa wikang Ingles). Hulyo 11, 2016. Nakuha noong Enero 25, 2021.
{{cite web}}: CS1 maint: date auto-translated (link)


