Carbon monoxide
Ang monoksidong karbono o Carbon monoxide (CO) ay isang walang kulay, walang amoy at walang lasang gaas na katamtamang mas magaan sa hangin. Ito ay nakakalason sa mga tao at hayop kapag naenkwentro sa mas mataas na mga konsentrasyon bagaman ito ay nililikha rin sa normal na metabolismo ng mga hayop sa mababang mga kantidad at pinaniniwalang may ilang mga tungkuling normal na pang-biolohiya. Sa atmospero, ito ay nagbabago sa espasyo, may maikling buhay at may papel sa pagkakabuo ng lebel sa lupaing osono. Ang monoksidong karbono ay binubuyo ng isang atomong karbono at isang atomong oksiheno na kinawin ng tripleng kawing na binubuo ng dalawang mga kawing na kobalente gayundin ng isang datibong kawing na kobalente. Ito ang pinakasimpleng oksokarbono at isoelektroniko sa ionong siyanuro at nitrohenong molekular]]. Sa mga kompleks na koordinasyon, ang ligandong monoksidong karbono ay tinatawag na karbonilo. Ang monoksidong karbono ay nalilikha mula sa parsiyal na oksidasyon ng naglalaman ng karbonong mga kompuwestong kimikal. Ito ay nabubuo kapag walang sapat na oksiheno upang lumikha ng dioksidong karbono (CO2) gaya ng pagpapaapoy ng isang kalan o isang panloob ng kombustiyong motor sa isang saradong espasyo. Sa presensiya ng oksiheno, ang monoksidong karbono ay nasusunog sa isang apoy na asul na lumilikha ng dioksidong karbono.[1] Ang gaas na coal na malawakang ginagamit bago ang mga 1960 para sa pagiilaw na pambahay, pagluluto at pagpapainit ay malaking binubuo ng monoksidon gkarbono. Ang ilang mga proseso sa modernong teknolohiya gaya ng pugong pang-apoy ay lumilika ng monoksidong karbono bilang subprodukto nito.[2]
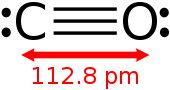
| |||
| |||
| Mga pangalan | |||
|---|---|---|---|
| Ninais na pangalang IUPAC
Carbon monoxide | |||
| Mga ibang pangalan
Carbon monooxide
Carbonous oxide Carbon(II) oxide Carbonyl | |||
| Mga pangkilala | |||
Modelong 3D (JSmol)
|
|||
Reperensya sa Beilstein
|
3587264 | ||
| ChEBI | |||
| ChemSpider | |||
| Infocard ng ECHA | 100.010.118 | ||
| Bilang ng EC |
| ||
Reperensya sa Gmelin
|
421 | ||
| KEGG | |||
| MeSH | Carbon+monoxide | ||
PubChem CID
|
|||
| Bilang ng RTECS |
| ||
| UNII | |||
| Bilang ng UN | 1016 | ||
Dashboard ng CompTox (EPA)
|
|||
| |||
| |||
| Mga pag-aaring katangian | |||
| CO | |||
| Bigat ng molar | 28.010 g/mol | ||
| Hitsura | colourless gas | ||
| Amoy | odorless | ||
| Densidad | 789 kg/m3, liquid 1.250 kg/m3 at 0 °C, 1 atm 1.145 kg/m3 at 25 °C, 1 atm | ||
| Puntong natutunaw | −205.02 °C (−337.04 °F; 68.13 K) | ||
| Puntong kumukulo | −191.5 °C (−312.7 °F; 81.6 K) | ||
Solubilidad sa tubig
|
27.6 mg/1 L (25 °C) | ||
| Solubilidad | soluble in chloroform, acetic acid, ethyl acetate, ethanol, ammonium hydroxide, benzene | ||
Repraktibong indeks (nD)
|
1.0003364 | ||
Momento ng dipolo
|
0.122 D | ||
| Termokimika | |||
Pamantayang entropiyang
molar (S⦵298) |
198 J·mol−1·K−1 | ||
Pamantayang entalpya
ng pagbuo (ΔfH⦵298) |
−110.5 kJ·mol−1 | ||
| Mga panganib | |||
| NFPA 704 (diyamanteng sunog) | |||
| Punto ng inplamabilidad | −191 °C (82.1 K; −311.8 °F) | ||
| Mga kompuwestong kaugnay | |||
Maliban kung saan nabanggit, binigay ang datos para sa mga materyales sa kanilang estadong pamantayan (sa 25 °C [77 °F], 100 kPa).
| |||
Sa buong mundo, ang pinakamalaking pinagmumulan ng monoksidong karbono ay nagmumula sa kalikasan dahil sa mga reaksiyong potokimikal sa tropospera na lumilkha ng mga 5 x 1012 kilogramo kada taon.[3] Ang ibang mga pinagmumulan ng CO ay mga bulkan, mga kagubatan, mga apoy sa kagubatan at ibang mga anyo ng kombustiyon. Sa biolohiya, ang monoksidong karbono ay likas na nalilikha ng aksiyon ng oksihenaseng heme 1 at 2 sa heme mula sa pagkasira ng hemoglobin. Ang prosesong ito ay lumilikha ng carboxyhemoglobin sa mga normal na tao kahit pa hindi sila humihinga ng anumang monoksidong karbono.
Mga sanggunian
baguhin- ↑ Carbon Monoxide – Molecule of the Month, Dr Mike Thompson, Winchester College, UK.
- ↑ Robert U. Ayres, Edward H. Ayres (2009). Crossing the Energy Divide: Moving from Fossil Fuel Dependence to a Clean-Energy Future. Wharton School Publishing. p. 36. ISBN 0-13-701544-5.
{{cite book}}: CS1 maint: date auto-translated (link) - ↑ Weinstock, B.; Niki, H. (1972). "Carbon Monoxide Balance in Nature". Science. 176 (4032): 290–2. Bibcode:1972Sci...176..290W. doi:10.1126/science.176.4032.290. PMID 5019781.
{{cite journal}}: CS1 maint: date auto-translated (link)